Caso clínico:

Um paciente precisando fazer cirurgia bariátrica, com peso muito acima do desejável para cirurgia segura, começou um tratamento com anfepramona 25mg (Dualid), visando perder, pelo menos, 30 kg no período de 2 meses. Passados 1 mês de tratamento, com redução de peso de 10 kg, o medicamento não correspondia mais ao efeito desejado. Em nova visita ao médico, este aumentou a dose do medicamento para 75 mg, voltando o medicamento a fazer efeito. Com base neste relato, o paciente pode ter desenvolvido taquifilaxia ou tolerância?
Para respondermos, precisamos compreender melhor o que é Taquifilaxia e Tolerância medicamentosa.
Tolerância medicamentosa
É a diminuição do efeito de uma medicação por exposição excessiva do paciente ao seu princípio ativo.
Diz-se que a tolerância a drogas se desenvolve quando se torna necessário aumentar a dosagem da droga para atingir o mesmo nível de efeito terapêutico que era alcançado quando a droga foi introduzida pela primeira vez. A tolerância pode acompanhar a dependência da droga ou pode ter uma significância farmacoterapêutica especial quando é de natureza farmacodinâmica (envolvendo uma reduzida capacidade de resposta dos receptores) ou farmacocinética (envolvendo uma taxa aumentada de biotransformação). Por exemplo: morfina e drogas relacionadas, drogas bloqueadoras de adrenalina que são usadas no tratamento da hipertensão.
Taquifilaxia
Uma tolerância aguda aos efeitos de uma droga, devida a uma causa farmacodinâmica que se desenvolve rapidamente, é denominada taquifilaxia.
A taquifilaxia em farmacologia é nome dado ao fenômeno de rápida diminuição do efeito de um fármaco em doses consecutivas. É a tolerância desenvolvida após poucas doses absorvidas do produto, por depleção do mediador disponível.
Então, o que você acha que aconteceu com o paciente?
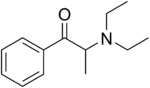 |
| (RS)-2-diethylamino-1-phenyl-propan-1-one |
A anfepramona (cloridrato), também conhecida como dietilpropiona, é um fármaco anorexígeno, auxiliar no tratamento da obesidade. Possui atividade similar mas de menor potência estimulante à anfetamina e trata-se de uma amina simpaticomimética.
A anfepramona tem ação no Sistema Nervoso Central. Produz efeito anorexígeno-saciogênico ao atuar no centro hipotalâmico da saciedade. Além disso, provoca estímulo no SNC, pode elevar a pressão arterial e produz efeito de tolerância. Em associação com uma dieta alimentar ficou estabelecido ser mais eficaz que a administração de uma dieta e placebo.
Atua na liberação da noradrenalina. Este, age nos núcleos hipotalâmicos laterais inibindo a fome. Tem potencial de dependência e gera tolerância (são necessárias doses maiores com o passar do tempo para obter o mesmo efeito), além de alterações psíquicas.
O efeito do medicamento diminui com seu uso.
Fonte:
- http://www.portaleducacao.com.br/farmacia/artigos/12465/dessensibilizacao-e-taquifilaxia#ixzz2NFfNcYD4
- http://www.areaseg.com/toxicos/toxicologia.html
é a espécie que perde elétrons (oxidou), é o agente redutor.
é a espécie que ganha elétrons (reduziu), é o agente oxidante.








